Syndrome myélodysplasique
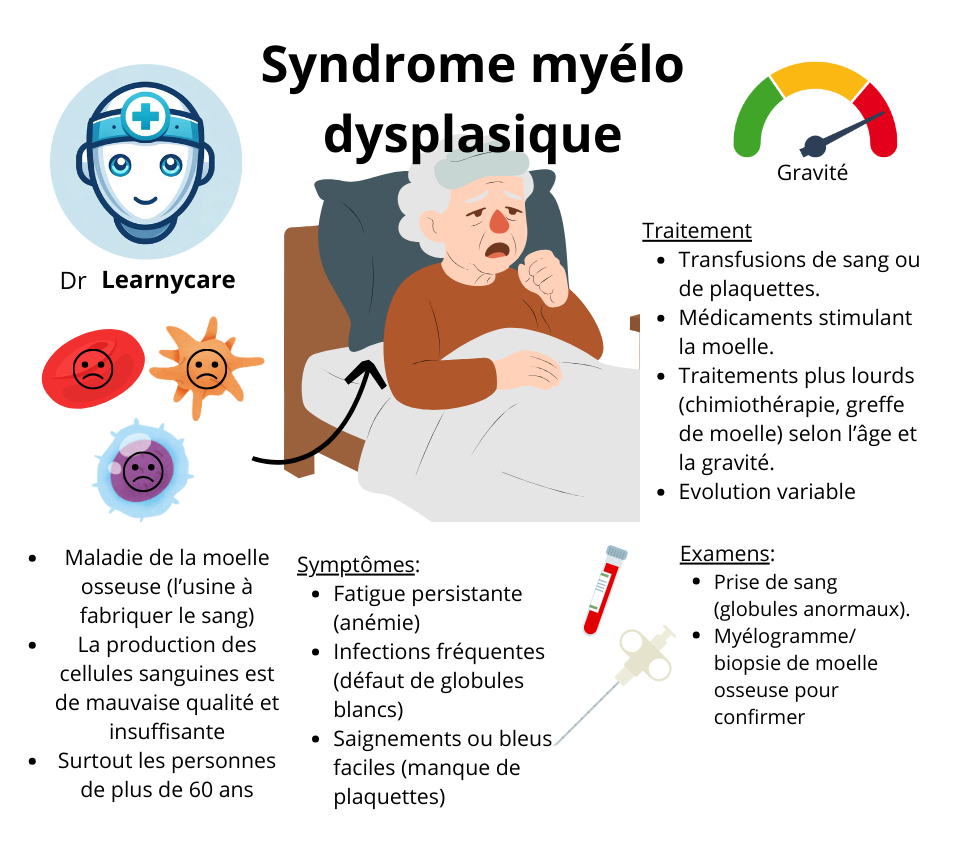
Lorsque nous pensons à notre santé, nous tenons souvent pour acquis le travail incroyablement complexe et délicat que nos cellules effectuent chaque jour. Chaque seconde, dans la moelle osseuse au cœur de nos os, des milliers de nouvelles cellules sanguines sont produites pour remplacer celles qui ont terminé leur cycle de vie. Mais que se passe-t-il lorsque ce processus remarquablement régulier déraille ? Entrez dans le monde mystérieux du syndrome myélodysplasique, une série de troubles qui surviennent lorsque la moelle osseuse ne produit pas suffisamment de cellules sanguines saines. Cette affection, qui touche généralement les personnes âgées, peut rester silencieuse pendant des années, ne se révélant que lorsque des symptômes tels que la fatigue, l’essoufflement ou les infections fréquentes commencent à perturber la vie quotidienne. Pire encore, dans certains cas, elle peut évoluer vers une leucémie aiguë, un type de cancer du sang particulièrement agressif.
Mais ne vous y trompez pas : le syndrome myélodysplasique n’est pas une maladie sans espoir. De nouvelles avancées dans la recherche médicale offrent des perspectives prometteuses pour la détection précoce, le traitement et peut-être même la prévention de cette maladie. Dans cet article, nous allons démystifier le syndrome myélodysplasique, explorer ses causes, ses symptômes, ses traitements, et mettre en lumière comment les avancées récentes pourraient changer la vie des personnes atteintes de cette maladie.
 Qu’est-ce que ?
Qu’est-ce que ?
Définition
Le syndrome myélodysplasique est une maladie acquise qui affecte une cellule essentielle de notre corps appelée la cellule souche hématopoïétique. C’est cette cellule qui, logée dans la moelle osseuse, donne naissance à toutes les différentes cellules sanguines que notre corps a besoin pour fonctionner correctement.
Dans le syndrome myélodysplasique, des changements génétiques malheureux affectent ces cellules souches. Parfois, il s’agit de mutations des gènes qui régulent l’épigénétique – la façon dont notre ADN est lu et utilisé – et l’épissage – comment l’information génétique est assemblée. Ces mutations conduisent à une “apoptose”, un terme scientifique pour désigner la mort programmée de la cellule. Cela résulte en une production insuffisante de cellules sanguines saines, un phénomène connu sous le nom de “cytopénie”.
Les problèmes causés par le syndrome myélodysplasique sont doubles. D’une part, il y a une pénurie de cellules sanguines, conduisant à des symptômes comme l’anémie, une diminution du nombre de plaquettes sanguines (thrombopénie), et une diminution des globules blancs (neutropénie). D’autre part, les cellules sanguines qui sont produites sont souvent anormales dans leur forme et leur fonctionnement.
Finalement, l’un des dangers les plus importants de ce syndrome est qu’il peut évoluer en une forme agressive de cancer du sang appelée leucémie aiguë myéloïde. C’est pourquoi comprendre, diagnostiquer et traiter rapidement le syndrome myélodysplasique est si crucial.
 Diagnostic
Diagnostic
Les personnes concernées
Le syndrome myélodysplasique est une maladie qui affecte relativement peu de personnes, avec une incidence d’environ 4 cas par 100 000 habitants chaque année. Toutefois, cette incidence est loin d’être uniforme à travers les tranches d’âge. En fait, cette maladie touche principalement les personnes âgées, avec un âge médian de diagnostic entre 65 et 70 ans.
Il est important de noter que l’incidence du syndrome myélodysplasique augmente considérablement avec l’âge. Pour ceux qui sont âgés de 70 à 80 ans, le taux grimpe à environ 70 cas par 100 000 habitants par an. Cela souligne l’importance d’une surveillance régulière de la santé, en particulier pour les personnes plus âgées.
Facteurs de risque
Le syndrome myélodysplasique est souvent une maladie mystérieuse qui semble surgir sans cause apparente. Cependant, nous avons identifié certains facteurs de risque qui peuvent augmenter la probabilité de développer ce trouble.
Traitements anticancéreux : certaines formes de chimiothérapie, en particulier celles qui impliquent une utilisation prolongée de médicaments spécifiques tels que les agents alkylants et les analogues de purines, peuvent augmenter le risque de syndrome myélodysplasique. Le syndrome peut se développer plusieurs années après la fin du traitement.
Exposition aux toxiques : certains produits chimiques, comme le benzène, souvent rencontré dans certaines situations professionnelles, peuvent augmenter le risque de ce syndrome. De même, le tabac contient des substances qui pourraient être liées à la maladie.
Radiations : une exposition importante aux radiations, que ce soit dans un contexte professionnel ou suite à des essais nucléaires, peut également augmenter le risque.
Autres maladies du sang : certaines maladies du sang acquises, comme les syndromes myéloprolifératifs, l’aplasie médullaire et l’hémoglobinurie paroxystique nocturne, peuvent également augmenter le risque de syndrome myélodysplasique.
Facteurs génétiques : enfin, certaines affections génétiques, notamment la trisomie 21 et des troubles rares comme l’anémie de Fanconi, la neutropénie de Kostmann et la neurofibromatose, peuvent également augmenter le risque. Ces facteurs génétiques sont particulièrement pertinents dans le cas du syndrome myélodysplasique chez l’enfant, où ils représentent environ un tiers des cas.
Rappelons que même si ces facteurs peuvent augmenter le risque de développer le syndrome myélodysplasique, beaucoup de personnes atteintes de ce syndrome n’ont aucun de ces facteurs de risque apparents. De plus, avoir un ou plusieurs de ces facteurs de risque ne signifie pas nécessairement qu’une personne développera la maladie. Il est toujours important de discuter de vos risques spécifiques avec un professionnel de la santé.
Les symptômes
Le syndrome myélodysplasique est une maladie sournoise qui peut ne pas produire de symptômes notables jusqu’à ce que le nombre de cellules sanguines saines diminue de manière significative. Lorsque les symptômes apparaissent, ils peuvent varier en fonction du type et du nombre de cellules sanguines affectées.
Parmi les symptômes les plus communs, on trouve ceux associés à l’anémie, comme la fatigue, la pâleur et l’essoufflement. En raison du faible nombre de plaquettes sanguines, les patients peuvent également présenter des symptômes hémorragiques, comme des saignements ou des ecchymoses facilement. Enfin, un faible nombre de globules blancs peut rendre les patients plus susceptibles aux infections.
Les signes
Les signes cliniques du syndrome myélodysplasique sont généralement subtils. Les patients ne présentent généralement pas de gonflement des ganglions lymphatiques. Cependant, un agrandissement de la rate pourrait être un signe du syndrome myélodysplasique, bien que cela puisse également suggérer d’autres troubles du sang.
Il est important de noter que ces symptômes peuvent également être causés par d’autres affections médicales. Si vous ressentez l’un de ces symptômes, il est important de consulter un professionnel de la santé pour un diagnostic et un traitement appropriés.
Les examens
NFS : cette analyse révèle souvent une anémie, c’est-à-dire un faible nombre de globules rouges. Ces globules rouges peuvent être de taille normale ou plus grands que d’habitude (macrocytaire), et contiennent une quantité normale d’hémoglobine (normochrome). De plus, le corps n’est pas capable de produire de nouvelles cellules sanguines pour remplacer celles qui sont perdues (arégénérative). Les patients peuvent également avoir un faible nombre de plaquettes (thrombopénie) et de globules blancs (leucopénie).
Frottis sanguin : un frottis sanguin, qui est une observation microscopique des cellules sanguines, peut révéler d’autres anomalies. Les globules rouges peuvent présenter une forme irrégulière (poïkylocytose), être plus grands que la normale (macrocytose), varier en taille (anisocytose) et présenter des taches basophiles. Les globules blancs peuvent montrer une dégranulation et une diminution de la segmentation. Les plaquettes peuvent être plus grandes ou plus petites que la normale. De plus, de petites quantités de blastes, des cellules sanguines immatures, peuvent être présentes.
Bilan de Möelle
Myélogramme : cet examen permet d’observer directement les cellules de la moelle osseuse, où les cellules sanguines sont produites. Il est généralement réalisé avec une coloration spéciale appelée coloration de Perls, qui aide à détecter l’excès de fer dans les cellules. Dans le syndrome myélodysplasique, la moelle osseuse est souvent riche en cellules, mais ces cellules sont produites de manière inefficace. Des anomalies morphologiques peuvent être observées dans les globules rouges, les plaquettes et les globules blancs. En outre, le nombre de blastes, ou cellules sanguines immatures, est généralement inférieur à 20%.
Caryotype : il s’agit d’une analyse des chromosomes dans les cellules. Dans le syndrome myélodysplasique, il peut y avoir des anomalies chromosomiques qui fournissent des informations importantes sur la maladie.
Biopsie ostéomédullaire : dans certains cas, un échantillon de la moelle osseuse peut être prélevé pour un examen plus approfondi. Ce test est généralement réservé aux cas où la moelle osseuse est pauvre en cellules (ce qui est le cas dans environ 15% des cas de syndrome myélodysplasique) ou lorsque l’on soupçonne une fibrose de la moelle osseuse, une affection où la moelle osseuse est remplacée par du tissu fibreux.
Bilan spécifique
Bilan pré-thérapeutique : avant de commencer un traitement, certains tests peuvent être effectués. Par exemple, le taux de ferritine plasmatique peut être mesuré chez tous les patients qui auront besoin de transfusions sanguines pour prévenir une accumulation excessive de fer dans le corps, appelée hémochromatose post-transfusionnelle. De plus, le taux d’érythropoïétine (EPO) dans le sang peut être mesuré pour déterminer quels patients pourraient bénéficier de l’EPO recombinante, une hormone qui stimule la production de globules rouges.
Examens à visée pronostique : d’autres tests peuvent être réalisés pour aider à prédire l’évolution du syndrome myélodysplasique. Par exemple, on peut rechercher des mutations génétiques acquises, qui sont présentes dans environ 80% des cas de syndrome myélodysplasique. Bien que ces mutations ne soient pas spécifiques à cette maladie, elles peuvent influencer son évolution. De plus, un test appelé cytométrie de flux peut être utilisé pour rechercher des anomalies dans les antigènes de surface des cellules de la moelle osseuse, ce qui peut également donner des informations sur l’évolution probable de la maladie.
Classification
Le syndrome myélodysplasique est un terme qui englobe plusieurs sous-types de maladies, chacun ayant des caractéristiques et des symptômes particuliers. Voici une explication simplifiée :
Anémie réfractaire sidéroblastique idiopathique acquise (ARSIA) : dans ce sous-type, l’anémie (faible nombre de globules rouges) est le principal symptôme. Dans la moelle osseuse, il existe une sidéroblastose pathologique, où des inclusions de fer sont trouvées dans les mitochondries des globules rouges.
Anémie réfractaire sans excès de blastes (ARSEB) : ici, l’anémie est présente sans un nombre excessif de blastes supérieur à 19%, ou de cellules sanguines immatures.
Anémie réfractaire avec excès de blastes (AREB) : dans ce sous-type, l’anémie est accompagnée d’un nombre excessif de blastes. Si les blastes représentent plus de 19% des cellules sanguines, il peut y avoir une transformation en leucémie aiguë.
Leucémie myélo monocytaire chronique (LMMC) : ce sous-type se caractérise par une augmentation du nombre de monocytes (supérieurs à 1000/mm3), un type de globule blanc dans le sang. L’augmentation de la taille de la rate est souvent présente, et des anomalies peuvent être détectées dans la moelle osseuse.
Syndrome myélodysplasique avec délétion du chromosome 5q, ou “syndrome 5q-“ : ce sous-type est plus fréquent chez les femmes de plus de 60 ans. Il est caractérisé par une anémie avec des globules rouges plus grands que la normale qui n’est pas corrigée par la production de nouvelles cellules sanguines, et un nombre élevé de plaquettes. Des anomalies spécifiques peuvent être observées dans la moelle osseuse, et un traitement spécifique est disponible. Le pronostic pour ce sous-type est généralement bon.
Chaque sous-type a ses propres particularités et peut nécessiter des approches thérapeutiques différentes. Il est important de discuter avec votre médecin des détails de votre diagnostic et de votre plan de traitement.
 Le traitement
Le traitement
Étape 1 : prendre en charge
La prise en charge du syndrome myélodysplasique est généralement une approche collaborative impliquant différents professionnels de la santé. Voici comment chaque rôle peut contribuer à la gestion de la maladie :
Professionnels de santé de ville : les professionnels de santé de ville, comme les infirmières, les pharmaciens et les assistants médicaux, peuvent souvent être les premiers points de contact pour les patients. Ils peuvent fournir des conseils de base, aider à orienter les patients vers les bons services de santé et soutenir les patients tout au long de leur parcours de soins.
Médecin généraliste : les médecins généralistes jouent un rôle central dans le diagnostic et la gestion du syndrome myélodysplasique. Ils peuvent identifier les symptômes de la maladie, organiser les tests nécessaires pour le diagnostic et aider à coordonner les soins avec les autres professionnels de la santé impliqués dans la prise en charge du patient.
Hématologue : les hématologues sont des médecins spécialisés dans les maladies du sang. Dans le cas du syndrome myélodysplasique, ils peuvent fournir des avis spécialisés, aider à déterminer le meilleur plan de traitement et suivre l’évolution de la maladie.
Urgences : en cas de symptômes graves ou de complications aiguës du syndrome myélodysplasique, les services d’urgence peuvent fournir des soins immédiats.
Il est important pour les patients atteints du syndrome myélodysplasique de rester en contact régulier avec leur équipe de soins de santé et de signaler tout nouveau symptôme ou changement de leur état de santé.
Étape 2 : syndrome myélodysplasique à faible risque
Pour les personnes atteintes d’un syndrome myélodysplasique à faible risque, l’objectif principal du traitement est de gérer les symptômes et d’améliorer la qualité de vie. Voici une explication simplifiée des diverses approches de prise en charge :
Prise en charge de l’anémie.
Prise en charge de la thrombopénie.
Prise en charge de la neutropénie
Il est important de noter que chaque patient est unique et que le plan de traitement doit être individualisé en fonction des symptômes, de l’état de santé général et des préférences du patient. Il est également essentiel de maintenir une communication ouverte et régulière avec l’équipe médicale pour discuter de l’évolution des symptômes et de l’efficacité des traitements.
Étape 3 : syndrome myélodysplasique à haut risque
Pour les patients atteints d’un syndrome myélodysplasique à haut risque, le but du traitement est d’essayer de contrôler la maladie, de prolonger la survie et, dans certains cas, de tenter de guérir la maladie.
Le choix du traitement dépend de nombreux facteurs, dont l’âge, l’état de santé général, le stade de la maladie et les préférences du patient. Il est important de discuter avec l’équipe médicale des avantages et des inconvénients de chaque option afin de prendre une décision éclairée.
 Surveillance
Surveillance
L’évolution du syndrome myélodysplasique (SMD) peut varier considérablement d’un patient à l’autre, en fonction de nombreux facteurs, dont la sous-catégorie de SMD, l’état de santé général du patient, et les traitements reçus.
Le SMD peut entraîner des complications graves, notamment une anémie sévère, des hémorragies et des infections. De plus, environ 30% des cas peuvent évoluer vers une leucémie aiguë myéloïde (LAM) ou d’autres formes de leucémie.
Les patients atteints de SMD nécessitent une surveillance régulière, qui peut comprendre des tests sanguins réguliers, des contrôles de la fonction hépatique, et la surveillance des niveaux de ferritine pour détecter une éventuelle hémochromatose. Des examens cardiaques peuvent également être nécessaires.
Prévention
Il n’existe pas de méthodes de prévention spécifiques pour le syndrome myélodysplasique (SMD) étant donné qu’il s’agit souvent d’une maladie idiopathique, c’est-à-dire qu’elle survient sans cause connue. Cependant, des mesures de prévention générale peuvent être appliquées en fonction des facteurs de risque connus pour cette maladie :
Éviter l’exposition à certaines substances chimiques : certains agents chimiques, comme le benzène et certains types de pesticides, sont associés à un risque accru de SMD. Si possible, il est préférable d’éviter de travailler avec ou d’être exposé à ces substances.
Ne pas fumer : fumer est associé à un risque accru de nombreux types de cancer, y compris le SMD. Arrêter de fumer peut réduire ce risque.
Radiations : l’exposition à des radiations de haute énergie, comme celles utilisées dans la radiothérapie pour traiter le cancer, peut augmenter le risque de SMD. Les personnes qui ont subi une radiothérapie doivent être surveillées de près pour détecter tout signe de SMD.
Surveillance médicale pour les patients à risque : les personnes qui ont reçu une chimiothérapie ou qui ont une affection génétique qui augmente le risque de SMD doivent être surveillées de près par leurs médecins.
En dépit de ces précautions, la plupart des cas de SMD ne peuvent être évités car ils sont le résultat de changements dans les cellules qui se produisent spontanément et qui ne sont pas encore bien compris.
Aller plus loin
Fatigue, infections fréquentes… Et si c’était un syndrome myélodysplasique ? Découvrez les signes pour intervenir au plus tôt.









Laisse ton commentaire
Vous devez être connecté pour poster un commentaire.